Doxycycline
La doxycycline (DCI) est une molécule de la famille des cyclines utilisée comme médicament antibiotique. C'est une tétracycline semi-synthétique développée au début des années 1960 par Pfizer Inc. et commercialisée sous le nom Vibramycine (en anglais : Vibramycin). La Vibramycine fut autorisée par la FDA en 1967 et fut le premier antibiotique à spectre large à prise quotidienne de Pfizer Inc. La doxycycline est la substance active d'autres médicaments comme Monodox, Periostat, Vibra-Tabs, Doryx, Vibrox, Adoxa, Doxyhexal et Atridox. Elle est efficace sur les bactéries intracellulaires.
| Doxycycline | |
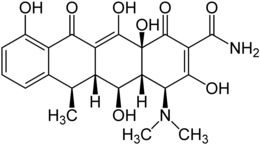
| |
| Identification | |
|---|---|
| Nom UICPA | (4S,4aR,5S,5aR,6R,12aS)-4-(diméthylamino)-3,5,10,12,12a-pentahydroxy-6-méthyl-1,11-dioxo-1,4,4a,5,5a,6,11,12a-octahydrotétracène-2-carboxamide |
| No CAS | |
| No ECHA | 100.008.429 |
| No CE | 209-271-1 |
| Code ATC | A01, J01 |
| DrugBank | DB00254 |
| PubChem | 11256 |
| ChEBI | 60648 |
| SMILES | |
| InChI | |
| Apparence | poudre cristalline jaune[réf. nécessaire] |
| Propriétés chimiques | |
| Formule | C22H24N2O8 [Isomères] |
| Masse molaire[1] | 444,434 6 ± 0,022 1 g/mol C 59,45 %, H 5,44 %, N 6,3 %, O 28,8 %, |
| Propriétés physiques | |
| T° fusion | 201 °C[réf. nécessaire] |
| Solubilité | 630 mg·L-1 eau à 25 °C[réf. nécessaire] |
| Écotoxicologie | |
| DL50 | 1 870 mg·kg-1 souris oral[réf. nécessaire] 241 mg·kg-1 souris i.v.[réf. nécessaire] 410 mg·kg-1 souris i.p.[réf. nécessaire] |
| Données pharmacocinétiques | |
| Biodisponibilité | 100 %[réf. nécessaire] |
| Métabolisme | Hépatique[réf. nécessaire] |
| Demi-vie d’élim. | 18-22 h[réf. nécessaire] |
| Considérations thérapeutiques | |
| Classe thérapeutique | antibiotique |
| Voie d’administration | Orale |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Usage
modifierElle est habituellement utilisée soit sous forme monohydrate ou sous la forme d'un sel (hyclate)[2].
On utilise cet antibiotique dans les affections suivantes :
- la syphilis (tréponème) ;
- les chlamydioses ;
- l'acné inflammatoire ;
- la maladie du charbon (Bacillus anthracis) ;
- le choléra (Vibrio cholerae) ;
- la peste (Yersinia pestis) ;
- la maladie de Lyme (Borrélies) ;
- la fièvre Q (Coxiella burnetii) ;
- la brucellose ;
- les infections à Mollicutes (Mycoplasma et Ureaplasma surtout) ;
- les gonococcies ;
- la pasteurellose ;
- les rickettsioses ;
- les infections à Haemophilus influenzae ;
- la tularémie.
La prophylaxie du paludisme[3] ainsi que de la maladie de Lyme[4] peuvent être dans certains cas du ressort de la doxycycline.
Effets indésirables
modifierLa doxycycline est un médicament globalement sûr, d'où sa large utilisation y compris en traitement chronique et prophylactique.
Néanmoins, il existe certaines contre-indications, en général les mêmes que pour les tétracyclines, notamment chez les patients atteints de lupus ou de troubles du foie, la doxycycline étant hépatotoxique et pouvant donc faire empirer voire provoquer une stéatose[5],[6],[7].
Elle a aussi parmi ses effets indésirables de pouvoir provoquer une photosensibilité (réaction chimique provoquée par la trop grande présence de substance photoréactive dans la peau et réagissant sous l'action des rayons UV ou visibles), ce qui peut être gênant dans le cas du traitement contre la malaria dans des pays très ensoleillés. Elle peut aussi provoquer, plus rarement, des mycoses buccales et génitales ; puisque la doxycycline se lie aux os et est hématotoxique, elle est à proscrire chez les femmes enceintes (troubles hépatiques, hernie inguinale potentielle chez le bébé) ou allaitantes ainsi que chez les enfants de moins de 8 ans (ralentissement réversible de la croissance osseuse et coloration jaune irréversible des dents avec un risque accru de caries). Les autres éventuels effets secondaires répertoriés sont : des maux de tête et nausées, diarrhées, maux de ventres, vomissements, troubles du sommeil, insomnies.
Enfin, il est recommandé de prendre la doxycycline au cours du repas du soir, au moins une heure avant de dormir, avec beaucoup d'eau et en position assise, car les comprimés restent facilement bloqués dans l'œsophage où ils peuvent provoquer des ulcères (généralement bénins mais douloureux).
Divers
modifierLa doxycycline fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[8].
Liens externes
modifier
- Ressources relatives à la santé :
- Notice dans un dictionnaire ou une encyclopédie généraliste :
- Compendium suisse des médicaments : spécialités contenant Doxycycline
Notes et références
modifier- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- The Merck Index, 33e édition (2001), pages 606-607, Merck research Laboratories
- (en) Frédéric Pagès et al., « Comparison of a doxycyclin monohydrate salt tolerability vs chloroquine-proguanil association in malaria chemoprophylaxis », Tropical Medicine and International Health, vol. 7, , p. 919-924 (ISSN 1365-3156).
- E.B. Hayes et J. Piesman, How can we prevent lyme disease, the New England Journal of Medicine, 18 septembre 2003, 348: 2424–2430
- Deboyser D, Goethals F, Krack G, Roberfroid M (1989). "Investigation into the mechanism of tetracycline-induced steatosis: study in isolated hepatocytes.". Toxicology and Applied Pharmacology. 97 (3): 473–9. . doi:10.1016/0041-008X(89)90252-4.
- Amacher DE, Martin BA (1997). "Tetracycline-induced steatosis in primary canine hepatocyte cultures.". Fundamental and Applied Toxicology. 40 (2): 256–63. . doi:10.1006/faat.1997.2389.
- Ekwall B, Acosta D (1982). "In vitro comparative toxicity of selected drugs and chemicals in HeLa cells, Chang liver cells, and rat hepatocytes.". Drug and Chemical Toxicology. 5 (3): 219–31. . doi:10.3109/01480548209041054.
- WHO Model List of Essential Medicines, 18th list, avril 2013